引言
转移性肿瘤的病理诊断,需结合临床、形态学及必要的特殊检查,后者如免疫组化。稍有经验的病理医师都会知道,敏感性和特异性俱佳的免疫组化指标并不多见,实际应用中必须警惕相关诊断陷阱。
推荐阅读
病理医师、病理技师、病理学教师、临床医师、肿瘤科医师、呼吸科医师、胸外科医师、规培学员、在校医学生、患者、健康人群。
简介
病理医师都知道,恶性黑色素瘤以“模拟”其他肿瘤的形态及免疫表型而臭名昭著。对于肺癌的组织病理诊断来说,免疫组化p40阳性是鳞状细胞癌的诊断基石,关于该抗体的应用陷阱极为罕见!不过,法国病理医师Thierry就曾在国际免疫组化及分子形态学会(International Society for Immunohistiochemistry & Molecular Morphology)官方期刊《Appl Immunohistochem Mol Morphol》杂志报告了一例恶性黑色素瘤转移至肺而表达p40的案例。为帮助大家更好的了解相关知识点并避免实际工作中的误诊误判,我们将该文要点编译介绍如下。
病例展示
患者66岁,既往吸烟,因脑部多发病变、考虑为出血性脑转移灶而入院。既往无恶性肿瘤病史。肺部发现一26mm肿物,CT引导下粗针穿刺活检。
组织学检查为恶性肿瘤,细胞具有非典型,无明显腺泡分化或鳞状分化;一处活检边缘可见胞质内色素颗粒。免疫组化检测,瘤细胞表达S-100、Melan-A、HMB-45及SOX10。
值得注意的是,80%的肿瘤细胞表达p40,且p40阳性的肿瘤细胞也表达前述黑色素标记。所有肿瘤细胞均不表达TTF-1。80%以上的肿瘤细胞表达AE1/AE3。相关免疫组化指标的检测均有阳性对照。
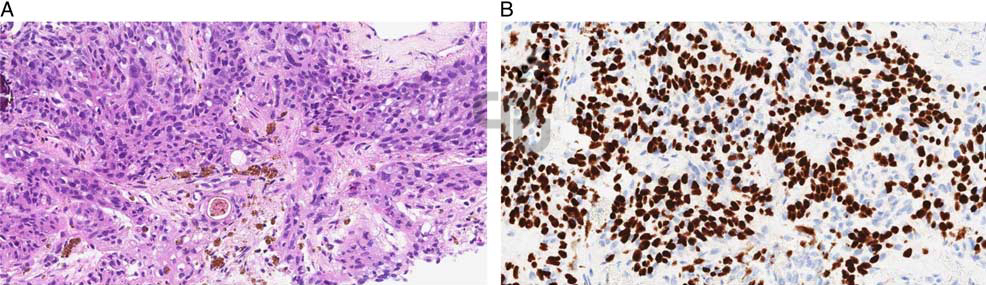
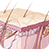
图1. 活检组织学所见;免疫组化表达p40(B)。
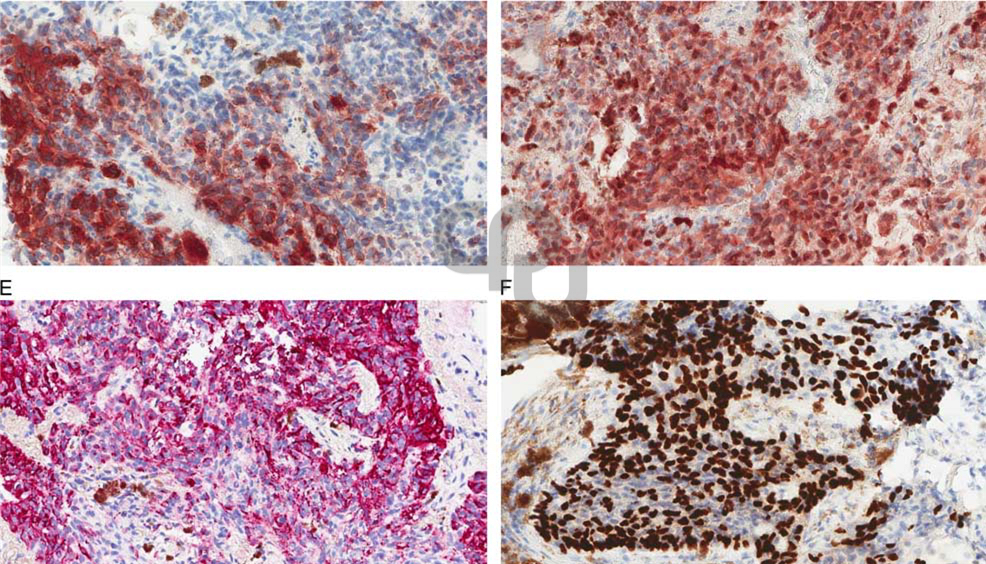
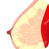
图2. 该肿瘤免疫组化还表达Melan-A(左上)、S-100(右上)、HMB-45(左下)、SOX10(右下)。
分子检测,证实BRAF的15号外显子有体细胞性c.1742A>C致病亚型,CDKN2A有c.283C>T种系点突变。因此本例最终诊断为转移性恶性黑色素瘤,伴p40异常表达。不过,仔细检查后,未见原发恶性黑色素瘤病灶。确诊数日后,患者去世。
小结
免疫组化p40对于肺鳞状细胞癌的诊断来说,高度特异且敏感;按照本文原作者所述,文献中尚无恶性黑色素瘤表达p40的报道,这应该是第一例相关报道。
虽然p40在肺腺癌鉴别诊断时的特异性接近100%,但该标记毕竟并不完全是鳞癌所特有。文献中有过鼻腔鼻窦小圆细胞肿瘤表达p40的报道,在嗅神经母细胞瘤、鼻腔鼻窦未分化癌、腺样囊性癌、INI1缺失型鼻腔鼻窦癌、原始神经外胚层肿瘤、Ewing肉瘤可有局灶阳性表达。文献中还有过乳腺分叶状肿瘤及转移性滋养叶细胞肿瘤表达p40的报道。
对于转移性恶性黑色素瘤的诊断来说,一般需要联合多种免疫组化标记。对于本例来说,黑色素标记均为阳性,强烈提示为恶性黑色素瘤。尤其HMB45和Melan-A更是高度特异。结合本例形态学可见黑色素颗粒的情况下,本无需做p40免疫组化。不过实际工作中,罕见情况下恶性黑色素瘤诊断中也要加做p40免疫组化,如鉴别皮肤梭形细胞肿瘤:有研究称,发生于皮肤的10例促纤维结缔组织增生型恶性黑色素瘤中,p40均为阴性。不过,恶性黑色素瘤可表达p63;MEK及RAF抑制剂治疗后的恶性黑色素瘤中p63是上调的。需要注意的是,p63抑制p53诱导的凋亡,因此可能在恶性黑色素瘤的靶向治疗耐药中发挥了一定作用。
P40属于p63的亚型之一,对于鳞状细胞癌的诊断来说,后者的特异性不如前者,阳性表达可见于淋巴瘤、多形性癌及某些滋养细胞肿瘤。对于胸部肿瘤来说,最近有报道称,p63和p40在NUT癌诊断中需要注意,前者可为弥漫阳性,而后者阴性、局灶阳性或弥漫阳性均有可能出现;SMARCA4缺陷型肿瘤中,p40一般为阴性或仅局灶表达;胸腺神经内分泌癌中一般并不表达p40;且除极罕见的情况外,p40和TTF-1一般不会出现共表达,因此实际工作中可以相互作为内对照。
本例分子检测证实BRAF的15号外显子有致病亚型,这一特征可见于肺腺癌和恶性黑色素瘤,在肺鳞癌中较为罕见。此外,其他分子检测结果更支持是恶性黑色素瘤。
全文完
参考文献
Thierry S, Juberthie B, Gyenes C, Dramais-Marcel D, Forest F. Challenging Metastatic Melanoma to the Lung With p40 Expression: A Diagnostic Pitfall, Case Report. Appl Immunohistochem Mol Morphol. 2023;31(1):64-67.
doi:10.1097/PAI.0000000000001083